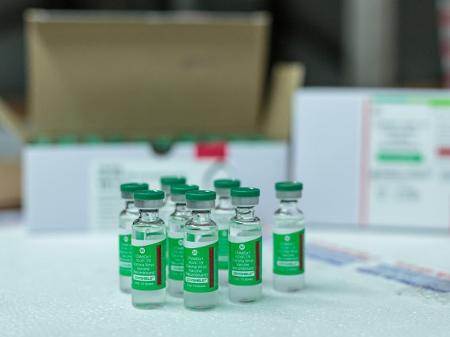
A Agência Nacional de Vigilância Sanitária (Anvisa) anunciou, nesta sexta-feira (12), a aprovação do registro definitivo da vacina de Oxford. A aprovação ocorre 42 dias após o pedido realizado pela Fundação Oswaldo Cruz (Fiocruz), no Rio de Janeiro, que produz o imunizante no País. Trata-se da segunda vacina contra a Covid-19 a obter o registro definitivo no País – a primeira foi a vacina da Pfizer, em 23 de fevereiro.
A agência também deu o aval para o primeiro medicamento para tratamento da Covid-19 no Brasil: o remdesivir. Inicialmente indicado para a evolução de pacientes com ebola, o remédio foi associado a uma recuperação mais rápida da forma grave da doença.
O registro permite a vacinação em massa e a comercialização do imunizante com o setor privado. A vacina de Oxford, desenvolvida pela Universidade de Oxford, no Reino Unido, e pela farmacêutica anglo-sueca AstraZeneca, integra o plano nacional de vacinação e está sendo aplicada por meio de uso emergencial desde janeiro em grupos prioritários no país.
O anuncio da Anvisa ocorre um dia depois que uma série de países suspenderam o uso da vacina de Oxford após suspeita de reação adversa grave, como trombose e embolia pulmonar. Dinamarca, Noruega, Bulgária, Romênia e Tailândia interromperam a aplicação do imunizante. Já Itália, Áustria e Luxemburgo suspenderam apenas alguns lotes da vacina. Na Espanha, algumas remessas do imunizantes estão em avaliação. No Brasil, não há registro de trombose nem de embolia pulmonar.